在实验室质量管理中,室间质量评价越来越受到临床实验室和实验室用户的重视。室间质量评价(external quality assessment,EQA)是多家实验室分析同一标本并由外部独立机构收集和反馈实验室的上报结果以评价实验室操作的过程。可在实验室中很多项目是没有EQA的,那实验室该如何保障这些项目的质量呢?
我国于2024年 5月 9 日发布了中华人民共和国卫生行业标准WS/T 415—2024《无室间质量评价时的临床检验质量评价》代替WS/T 415—2013《无室间质量评价时实验室检测评估方法》。

评价方法
分割样品比对——定量检验项目
定义与目的
本质:
将同一原始样本均分为多份,送至不同实验室检测。
核心作用:
● 评估实验室间检验结果一致性;
● 识别偶然误差与系统误差;
● 验证纠正措施有效性。
实施关键要求
样本特性:
● 均匀性&稳定性:需通过预实验验证(如不同批次分装一致性测试);
● 样本量:每次至少5份患者样本(浓度覆盖检测范围);
● 备用样本:需额外保留≥2份,用于异常结果复测。
质量控制标准
执行频率:
每半年至少1次(建议高风险项目缩短周期)。
结果判定(定量项目):
5 份样品中至少4份样品结果的百分差值或绝对差值在规定的范围(允许总误差)之内,认为比对结果可接受。
允许总误差(TE))制定依据:
● 生物学变异(参考CLIA指南);
● 当前室内质控水平;
● 实验室历史数据统计分析。
文件化管理
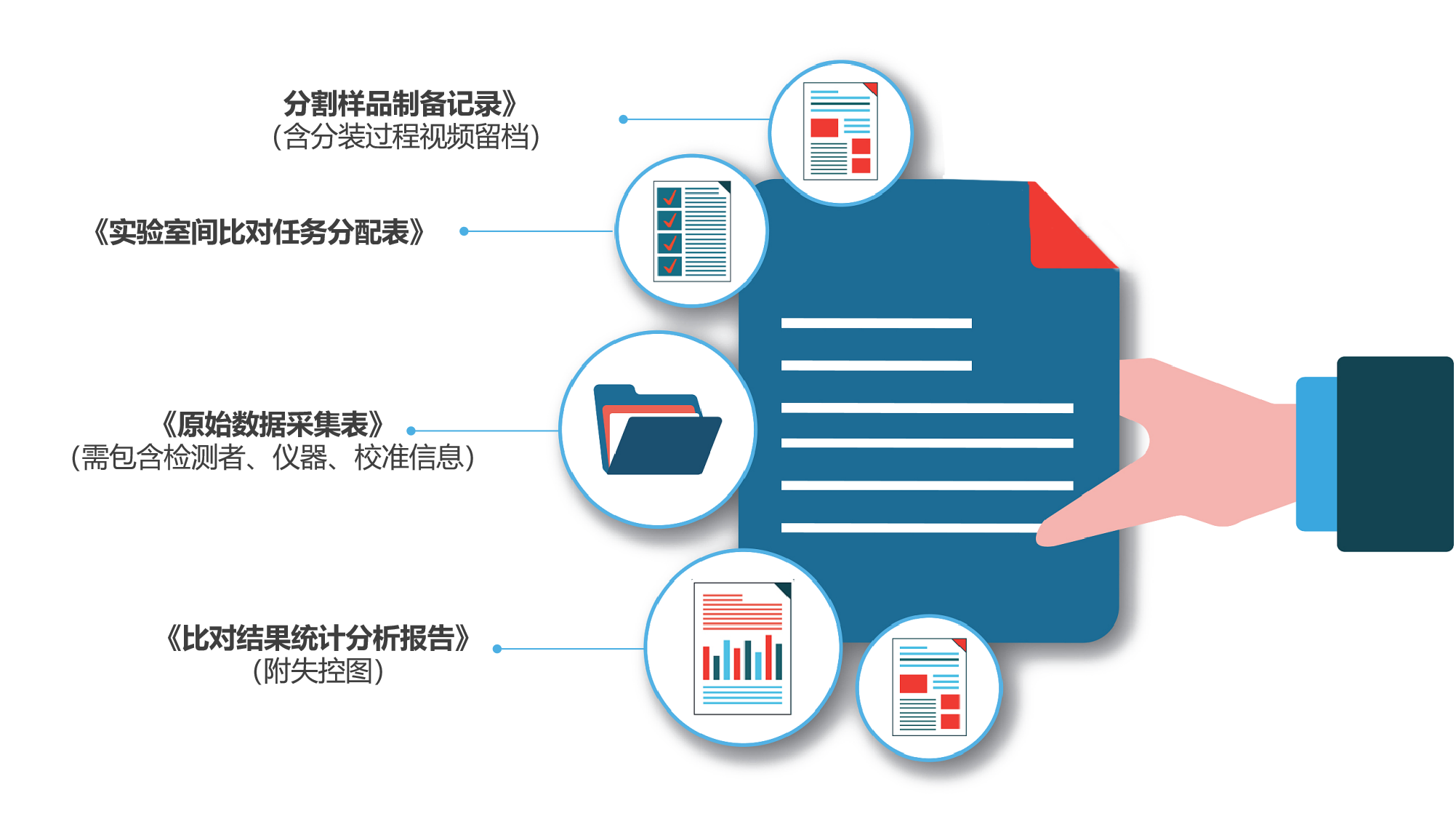
必备文档:
●《分割样品制备记录》(含分装过程视频留档)
●《实验室间比对任务分配表》
●《原始数据采集表》(需包含检测者、仪器、校准信息)
●《比对结果统计分析报告》(附失控图)
程序价值
合规保障:满足ISO 15189、CLIA 88等法规对室间质控的要求。
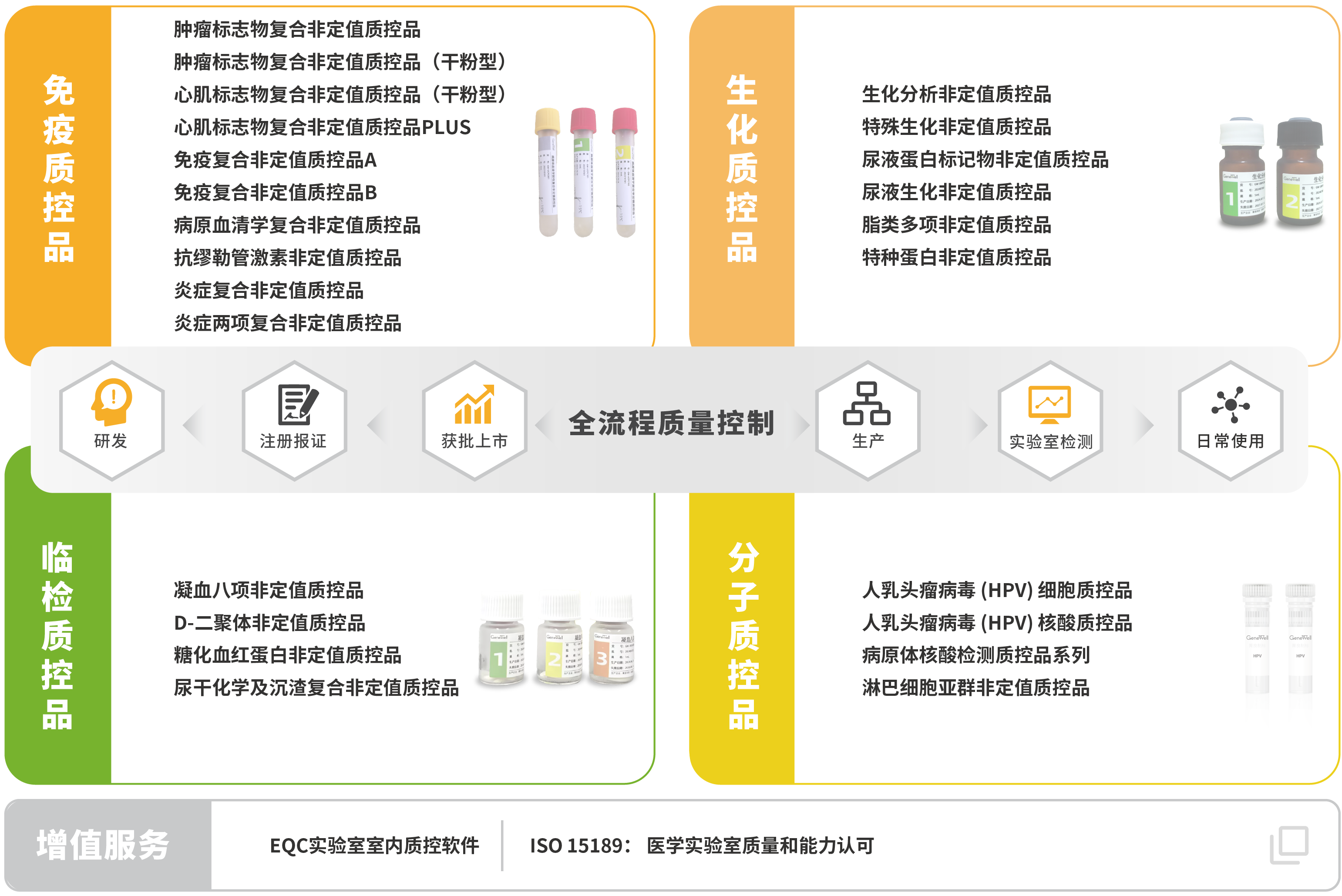
菁良临床质控一站式解决方案
菁良通过自主研发和国产化生产,向体外检测行业用户及合作伙伴提供全球领先的临床实验室质量控制解决方案,协助医学实验室实现全面质量管理。现已推出专业的质控管理软件及ISO15189质量管理体系咨询服务,第三方质控品涵盖免疫诊断、生化诊断、分子诊断等体外诊断细分领域。
关于菁良
菁良科技(深圳)有限公司是全球领先的提供体外诊断标准品与质控品的研发创新型高科技企业。
菁良通过自主研发的平台,向体外检测行业用户及合作伙伴提供全球领先的标准物质、第三方质控产品和企业参考品服务,助力提高行业检测准确率。参与多项由检测领域行业龙头和监管机构发起的标准制定工作,多次支持由临检中心发起的室间质量评价 (EQA)/能力验证项目。
菁良秉承着“精准制标,匠心良造”的理念,怀抱着“提高体外检测准确率,助力精准医学快速发展”的愿景,致力于建立规范化的中国体外检测金标准平台。
