凝胶电泳是许多分子生物学实验的重要部分。建立核酸电泳需采取一系列步骤来实现核酸样品的最佳分离和分析。核酸凝胶电泳工作流程中的关键步骤包括:
1.选择和制备凝胶
a.琼脂糖凝胶 b.聚丙烯酰胺凝胶 c.凝胶制备中的缓冲液选择
2.准备标准品和样品
a.核酸梯度选择 b.样品和梯度准备 c.加载染料和缓冲液选择
3.运行电泳
a.电泳缓冲选择 b.电压 c.电泳时间
4.在凝胶中可视化样品
a.荧光染色 b.紫外阴影
5.记录凝胶
a.荧光成像 b.射线自显迹法
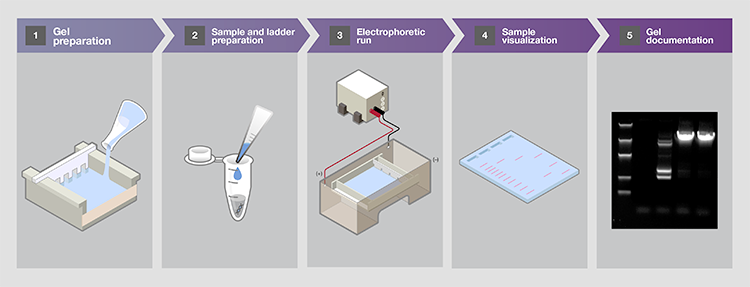
图1.核酸凝胶电泳的5大关键步骤。
1.选择和制备凝胶
琼脂糖(9012-36-6)和聚丙烯酰胺(9003-05-8)是核酸分离中最常用的两种凝胶基质。两种材料都是三维基质,孔径大小适合核酸分离,且与样品间无反应。可通过改变基质的百分比来调整孔径大小,从而有效分离不同大小的核酸。
有关琼脂糖凝胶和聚丙烯酰胺之间的选择,主要取决于核酸样品的大小和所希望达到的分辨率,虽然凝胶灌制和样品回收的方法也可考虑(表1)。琼脂糖凝胶的孔径大小非常理想,可分离0.1-25 kb范围内的核酸分子。聚丙烯酰胺形成的孔径较小,可用于分离小于1 kb的核酸分子。某些情况下,可采用聚丙烯酰胺凝胶以获得片段小于100bp的单碱基分辨率[1]。

a.琼脂糖凝胶
关于凝胶制备,琼脂糖凝胶通常以粉末形式提供,近年来也有方便的预称重片可供使用。为简化工作流程、节省时间,可考虑预制琼脂糖凝胶,其在某些 市售系统中作为集成单元来运行、可视化和分析。
制备您自己的琼脂糖凝胶,凝胶比例计算为:
凝胶%(w/v)=(琼脂糖g/缓冲液ml)x 100%
凝胶灌制时,如果使用了荧光核酸染色剂(溴化乙锭1239-45-8),可在凝胶灌制时加入推荐浓度(例如,溴化乙锭0.5 μg/mL)。
表2为不同长度的DN**段分离提供了推荐的琼脂糖凝胶百分比[2]。一般而言,较高比例的凝胶便于更小片段、更好的分离和分辨(图2)。注意,低比例凝胶十分脆弱且难以操作,而高比例凝胶则较浑浊,且会干扰可视化。
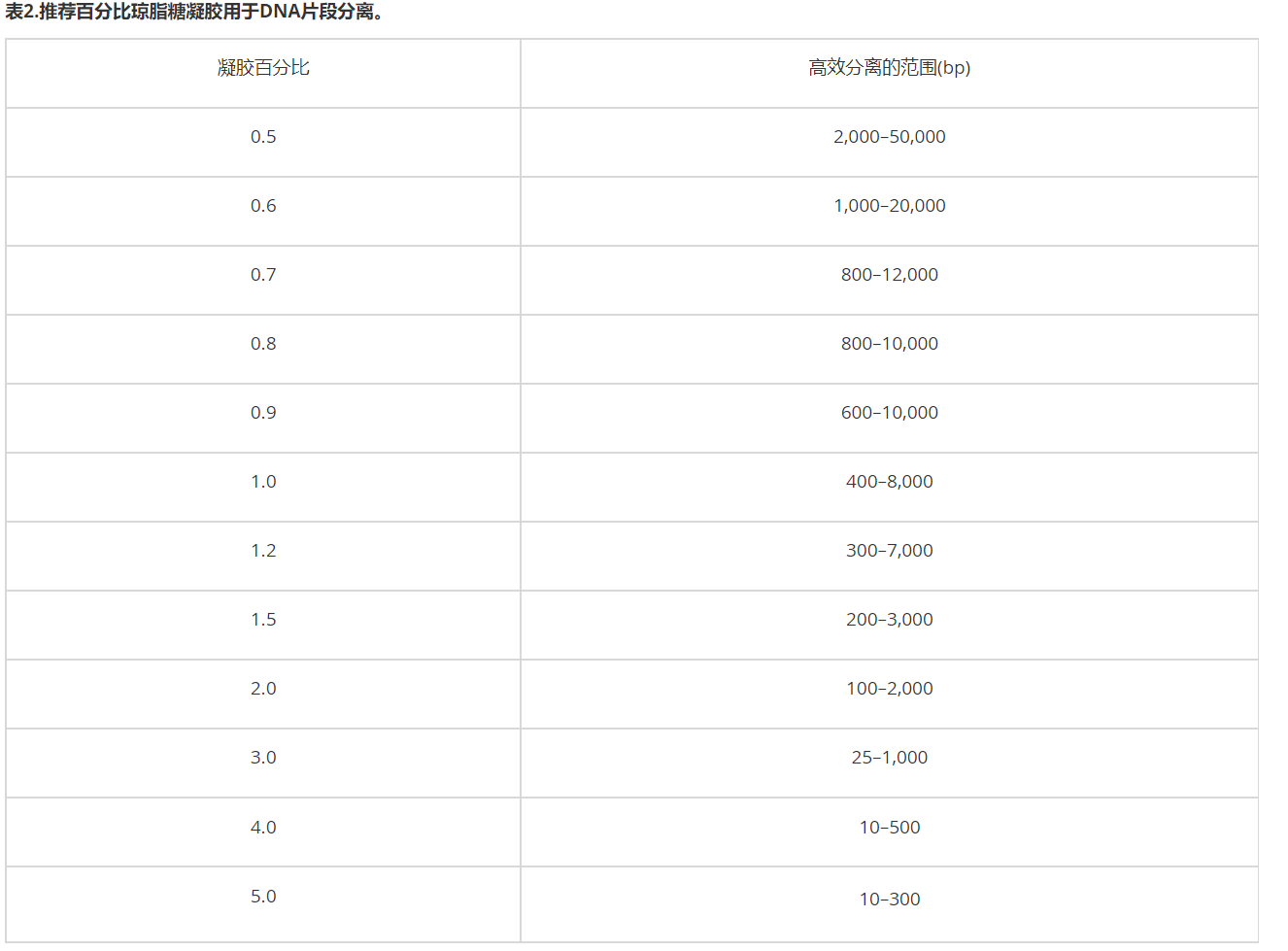
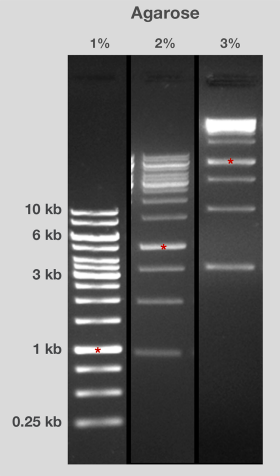
图2.不同百分比的琼脂糖凝胶中DN**段的流动性。在相同条件下(包括运行时间),在1%、2%和3%琼脂糖凝胶上分离出相同的DNA阶梯。1kb片段用红色星号表示,以供比较。
琼脂糖成分
琼脂糖是一种经过纯化的琼脂,是海洋红藻细胞壁的碳水化合物结构组成部分。 琼脂糖是一种分子量约为12万的无支链(线性)聚合物,含有800-1000个单糖。 琼脂糖链由一种重复的异二糖-即-D-半乳糖和3,6-酐-α-L-半乳糖通过1-4糖苷键结合而成。 双糖单位,也称琼脂二糖,通过a-1、3连接形成了一个链(图3)。
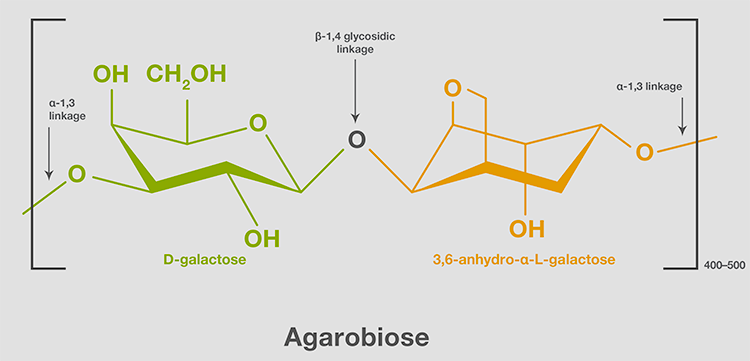
图3.琼脂糖的结构单元。琼脂糖由400-500个琼脂二糖单位组成。
琼脂糖溶液加热并冷却后,就会形成凝胶基质。其孔洞直径从50到200纳米不等,由凝胶浓度控制。温度高于90℃,琼脂糖便会融化,变成无规卷曲。冷却后,两个琼脂糖链形成由氢键连接的螺旋纤维。进一步冷却至胶凝固点以下(通常小于40°C),则会有更多氢键连接形成螺旋束网络,进而形成具有三维网格的凝胶(图4)[3,4]。 由于氢键,琼脂糖形成的凝胶加热可逆。因此,通过溶解含有目的片段的凝胶,可提取电泳分离出的核酸。
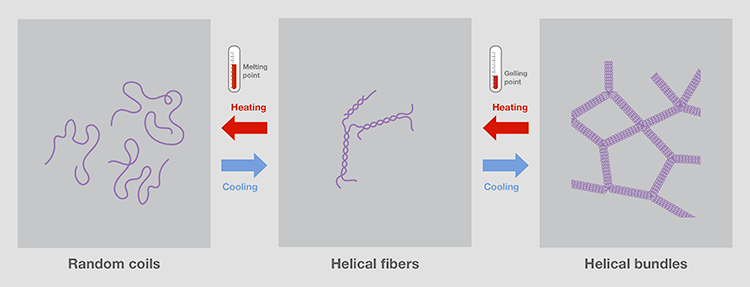
图4.通过加热和冷却改变溶液中琼脂糖的结构。
对大于10kbp DNA的提取,低熔点(LMP)的琼脂糖是较合适的选择。LMP琼脂糖在65度左右(1%的凝胶)融化—相对较低的温度,确保可以温和地提取凝胶中完整的核酸大分子。 LMP琼脂糖的低凝胶温度(~25°C)使其成为凝胶内酶反应的理想选择(例如,连接)。酶在半固态的琼脂溶液中处于活跃状态。
b.聚丙烯酰胺凝胶
聚丙烯酰胺-丙烯酰胺和交联剂—双丙烯酰胺(简称为“bis”)的组分-可以粉末形式提供,但为了方便通常预先制备成原液。该粉末和液体形式是为大家所知的神经毒素,应使用实验室防护性设施,小心操作。在凝胶中,丙烯酰胺和双丙烯酰胺(以%T表示)的总浓度决定了孔隙大小—通常直径为20-150纳米。百分比越高,孔隙越小,可分辨的分子也更小。表3展示了常用的凝胶比例[2]。
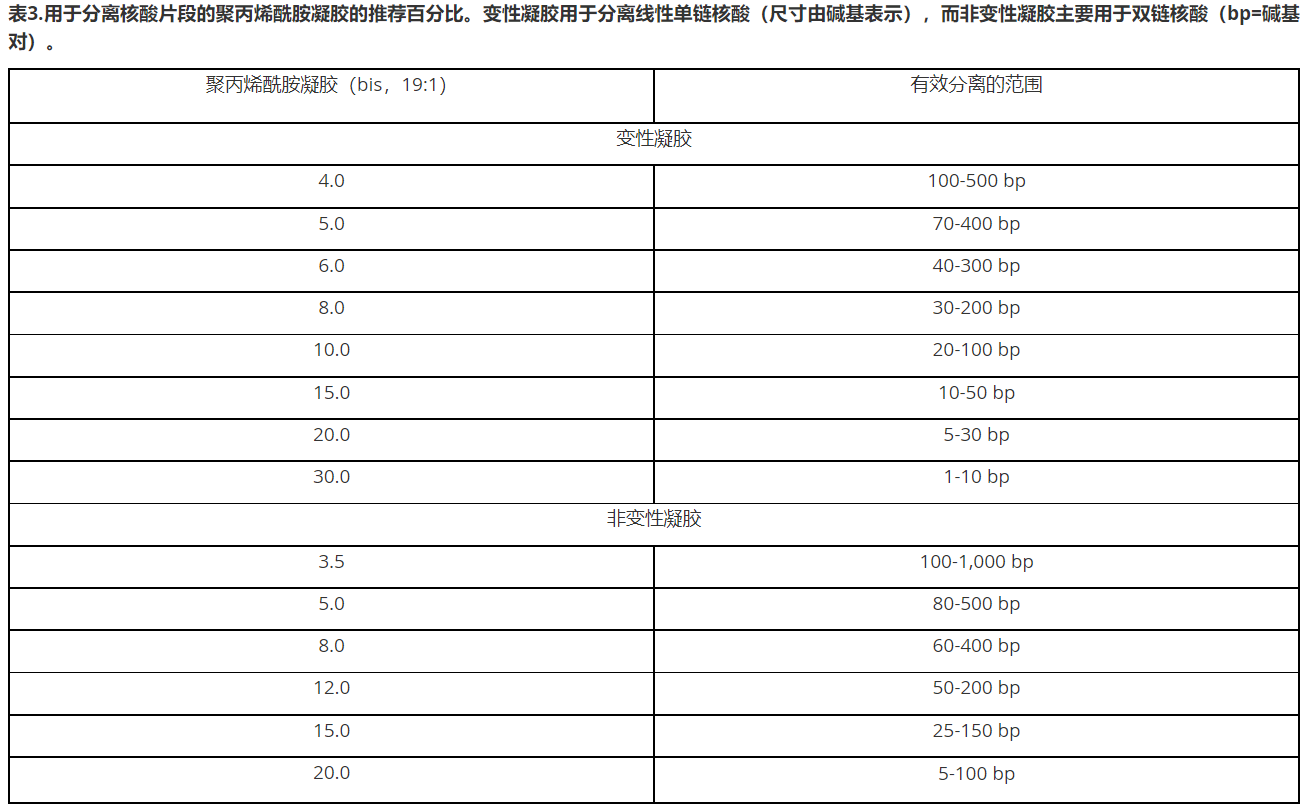
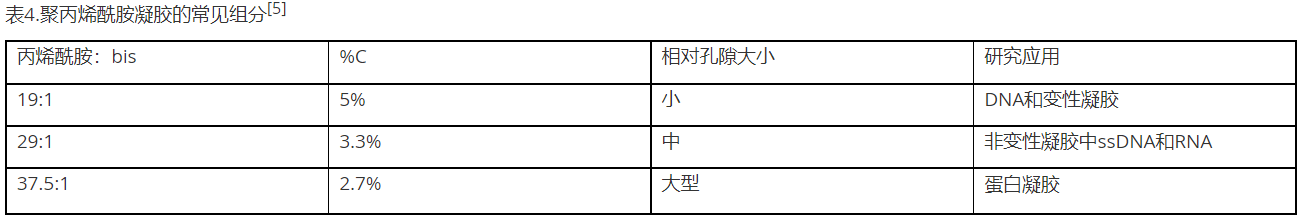
核酸分离,通常采用3–30%(%T)的聚丙烯酰胺凝胶。除%T之外,双丙烯酰胺(交联剂)与总丙烯酰胺(%C)的重量百分比是聚丙烯酰胺凝胶孔隙大小和样品分离的的关键(表4)。
%T和%C可以表示为:
%T(w/v)=[(丙烯酰胺+双丙烯酰胺)g/缓冲液ml]x 100%
%C(w/w)=[双丙烯酰胺g/(丙烯酰胺+双丙烯酰胺)g]x 100%
聚丙烯酰胺的基本原理
聚丙烯酰胺是由丙烯酰胺单体聚合而成的聚合物,通常与双丙烯酰胺或N,N'-亚甲基双丙烯酰胺结合使用。交联剂双丙烯酰胺含有两个单位通过亚甲基桥连的丙烯酰胺。聚合是被TEMED 催化(N,N,N′,N′-四甲基乙二胺)的自由基反应-通常由过硫酸铵(APS)引发(图 5)。因此,在既定温度下,APS和/或TEMED的浓度决定了聚合速率。
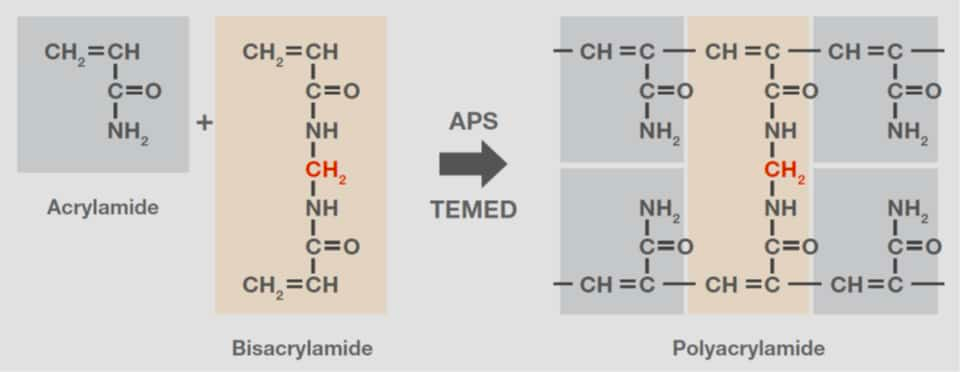
图5.丙烯酰胺形成聚丙烯酰胺,双丙烯酰胺结构展示。双丙烯酰胺含有两个单位通过亚甲基桥连的丙烯酰胺(红色)。
c.凝胶制备中的缓冲液选择
使用具有导电性的离子溶液制备琼脂糖和聚丙烯酰胺凝胶,确保核酸在电泳过程中具有迁移性。电泳过程中,凝胶和电泳缓冲液通常使用相同类型的缓冲液,以保持相同的pH值和离子强度。核酸电泳常用的两种缓冲液为Tris-醋酸盐EDTA (TAE)和Tris-硼酸盐EDTA (TBE),两者都有接近中性的pH值,有利于带负电荷的核酸。
为分析单链DNA或RNA,琼脂糖和聚丙烯酰胺凝胶通常在变性条件下制备和运行。变性条件会破坏核酸之间形成的氢键,从而减少像发夹环这样二级结构的形成。因此对RNA分离和分析而言,变性电泳更常用。琼脂糖和聚丙烯酰胺凝胶核酸电泳中常用的变性缓冲液包括:
琼脂糖:磷酸钠缓冲液中的乙二醛和DMSO、NaOH-EDTA缓冲液、MOPS缓冲液中的甲醛或甲酰胺等
聚丙烯酰胺: TBE缓冲液中的尿素
2.准备标准品和样品
a.核酸标准品选择
当运行凝胶时,含有已知大小的核酸参照样品通常被称为标准品、标记或 分子量标准,用于目的样品大小的估计。 在为给定样品选择合适的分子量标准时,需考虑如下因素:
Ladde类型(例如DNA或RNA),片段结构(例如单链或双链),构象(例如超螺旋、开环或线性)以确保对迁移进行适当比较
片段的数量和适当的分离形式,用于大小的估计
预期用途,如分子量标准是设计用于定性分析还是精确的定量测定
不同类型凝胶适用的分子量标准(例如,部分预制凝胶推荐设计 特定分子量标准以获得最佳运行结果)
上样染料的性质,避免目的条带模糊(图6)
上样缓冲液与使用凝胶的兼容性(例如,缓冲液的盐浓度会影响样品的迁移)
早期,DNA的大小标准主要来源于病毒基因组片段((例如,λφX174)和细菌质粒(如pUC19)的限制内切。该标准物在内切、样品纯度和电泳中带型的重现性方面存在问题。而后,从连接反应和/或PCR中获取的含有片段的分子量标准,因具有再现性且可产生预期大小的片段,而备受青睐。如今,因为色谱纯化片段实现了质量、带型、强度和数量等方面的更高控制,被视为分子量标准黄金标准(图6)。
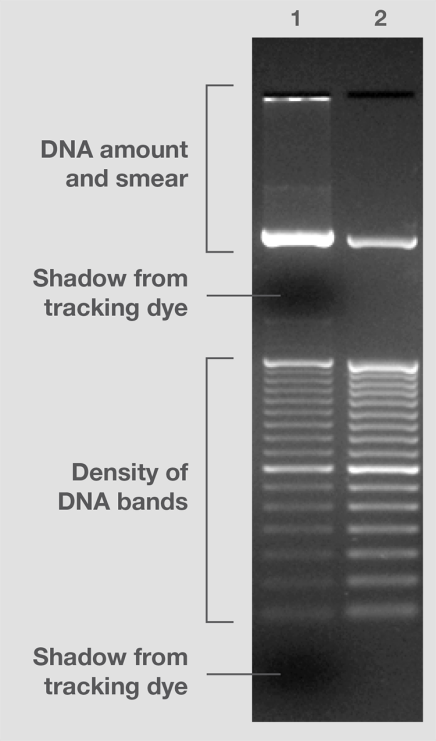
图6.DNA 分子量标准差异。 分子量标准 #2由色谱纯化的DN**段组成,存在于上佳的上样缓冲液中,可产生相等或预期强度的条带,并且不含有条带污点,无染色阴影。 与此相反,分子量标准 #1采用较老技术制造,并存在于次优组分的缓冲液中。
此外,还设计出室温下稳定、适合运输和储存,以及方便和少环境影响的分子量标准。而预混合,即用型分子量标准也可供选择—添加了最佳浓度、可直接上样到凝胶的上样染料的分子量标准。
注意,由不同制造商生产、描述相同(例如,1kb或100bp)的分子量标准,包含DN**段的数量、大小和密度可能会有所不同(图7)。使用前,请参考制造商提供的指南和协议,获取分子量标准组成及其使用用途准确而详细的说明。
与DNA分子量标准不同,RNA分子量标准通常与含有变性剂的上样缓冲液一同提供。变性剂可维持RNA的单链形式,确保样品可预测的迁移和分离结果。当运行RNA凝胶电泳时,应避免使用DNA分子量标准,因为双链分离,在变性条件下使用会导致非规则方式分离。

图7.两个不同供应商A和B,提供具有相同描述的DNA分子量标准片段组成差异。
b.样品和标准品准备
须计算上样到凝胶中的DNA量,以确保目的条带良好分离,并用于可视化和检测。虽然用荧光染料足以检测1-100ng/条带的DNA,但最小可检测量取决于所用染料[6]。注意,样品或标准品的超载会造成条带污点并遮盖附近条带,从而导致条带分辨不清,特别是片段大小相似时(图8A)。

图8.次优样品分离。 (A) 负载影响条带分辨率。 (B) 上样量过低会导致条带扭曲。
在上样缓冲液中准备好样品和分子量标准,其最终的体积通常占胶孔体积的30%。 由于孔底分布不均匀(图8B),使用较少的上样体积会导致条带扭曲。对于含有DNA结合蛋白或粘性末端的样品,凝胶上样之前,混合物需加入至含有SDS的上样染料中一同加热,因为蛋白质结合以及DN**段之间的相互作用会导致分离效果不佳(图10B)。
